
编译:公子欣
随着年龄的增长,细胞失去更新能力,便更易患癌,但关于衰老如何改变癌症的生物学,还有很多未知之处。日前,美国纪念斯隆凯特琳癌症中心(MSK)的一项研究提供了新的证据——对于癌症,衰老是一把双刃剑。在老年早期,癌症的发病率会提高;但在老年后期,衰老的基因组调控导致细胞干性下降,反而会抑制癌症的发生发展。研究在《自然》杂志上发表。

该研究第一作者Xueqian Zhuang博士指出,许多癌症类型都类似,大多数人在70岁左右被诊断出癌症,但一旦到了80或85岁,发病率又开始下降。但其中的原因一直未被揭示。

为了弄清楚为什么癌症发病率在老年早期达到顶峰,在老年后期反而开始下降,MSK研究小组研究了一种基因修饰的肺腺癌小鼠模型。肺腺癌是一种常见肺癌,约占全球癌症死亡人数的7%。
研究小组发现,随着年龄的增长,小鼠会产生更多的NUPR1蛋白质,会使肺部的细胞表现出缺铁的状态。
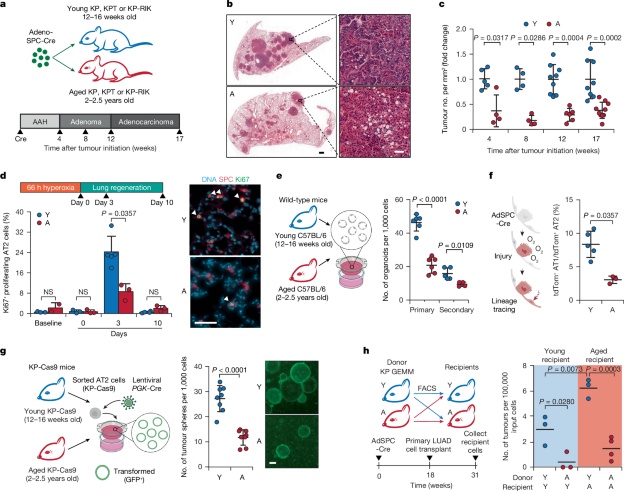
老化的AT2细胞表现出细胞再生和肿瘤发生的内在潜力降低
由于老年小鼠体内的细胞似乎没有足够的铁元素,失去了一些再生能力。而这种再生能力与癌症的发生直接相关,因此年长小鼠比年轻小鼠患癌症几率要小得多。值得注意的是,给老年小鼠补充额外的铁或减少细胞中NUPR1的数量,
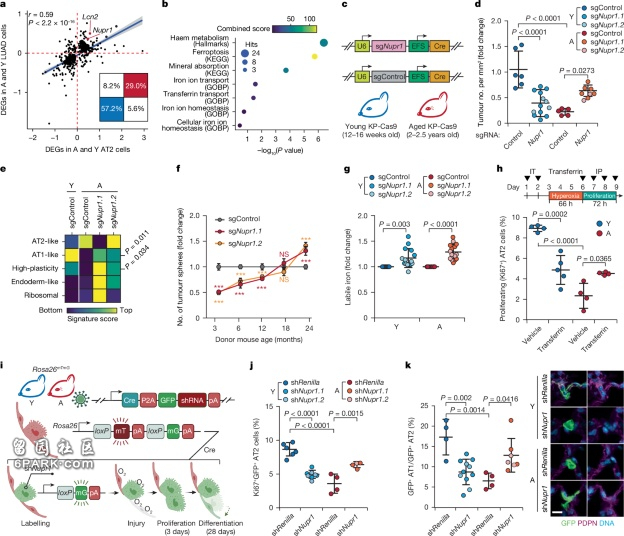
Nupr1的诱导通过破坏铁稳态来抑制老年肺中的肿瘤发生
“这一发现可能对人类有直接帮助,”MSK资深研究作者Tuomas Tammela博士说,“目前,特别是在新冠之后,由于肺部没有从感染中完全愈合,或者出于其他原因,许多人的肺功能不足。在小鼠身上的实验表明,补充铁可以帮助肺部再生,我们有很好的方法直接将药物输送到肺部,比如哮喘吸入器。”但这也是“双刃剑”性质发挥作用的地方。研究表明,
对针对铁代谢的治疗反应不同
研究小组的发现对基于一种叫做“铁死亡”(Ferroptosis)的细胞死亡的治疗也有重要意义,这种细胞死亡是由铁引发的。早在2012年,人们就发现了铁死亡,目前正在研究一些诱导铁死亡的小分子化合物以及之前获得FDA批准的药物,以研究其杀死癌细胞的潜力。
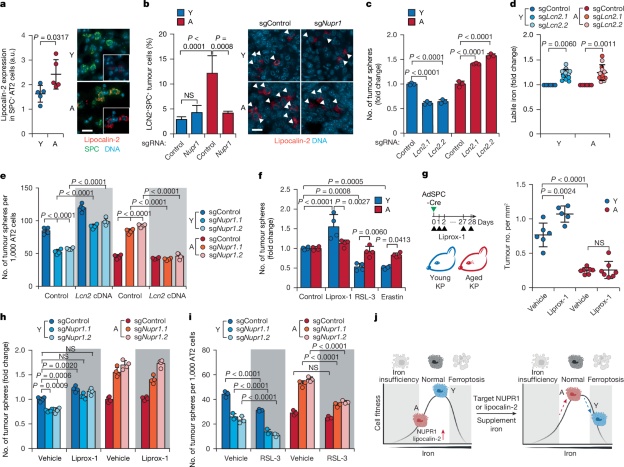
Nupr1通过脂质运载蛋白-2驱动衰老AT2细胞的功能性铁不足和铁死亡抵抗
研究人员发现,老年细胞比年轻细胞对铁死亡的抵抗力强得多,因为它们的功能就像没有足够的铁一样。这意味着针对铁死亡的治疗在老年患者中可能不如在年轻患者中有效。Tammela博士说:“我们在探索铁生物学的过程中发现,
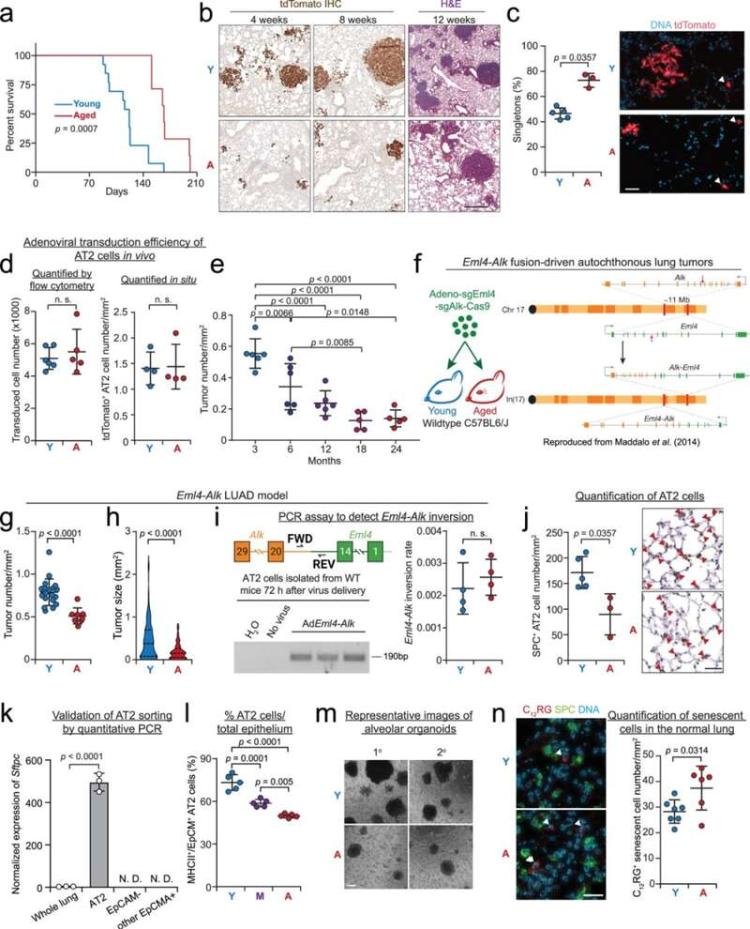
衰老通过降解起源细胞的干性来抑制肺肿瘤发生
庄博士补充说,“对我们来说,这说明细胞的生物学特性随着年龄的增长而变化,对药物的敏感性也会发生变化。因此,医生在临床试验中可能需要非常小心,例如,要观察老年和年轻患者的影响。”
Tammela博士表示,这项研究最终有一个更大的收获,“我们的数据表明,就癌症预防而言,年轻人当下所做的事情可能比老年人更危险。因此,在年轻时要防范吸烟、紫外线照射或接触其他明显的致癌物质,可能比我们想象的更为重要。”数据图及参考来源: